
Evolution und Regulierung der Biosynthese von Naturstoffen
In unserer Gruppe wollen wir (i) besser verstehen, wie Pflanzen wiederholt Wege entwickeln, um dieselbe Art von Naturstoffen zu produzieren, und (ii) neue Methoden anwenden und anpassen, um Stoffwechselwege und Regulierung auf zelltypspezifischer Ebene in Modell- und Nicht-Modellarten zu untersuchen.

Pflanzen produzieren eine enorme Vielfalt von Naturstoffen (spezialisierte Metaboliten). Während einige von ihnen einzigartig sind und nur in bestimmten Pflanzenlinien vorkommen, sind andere weiter verbreitet. Interessanterweise wurde in einigen Fällen die Biosynthese selbst komplexer Naturstoffe mehr als einmal in der Natur erfunden. Die Untersuchung solcher konvergent entwickelten Stoffwechselwege bietet nicht nur einzigartige Einblicke in die Evolution von Stoffwechselwegen, sondern kann auch als Grundlage für Ansätze zur Entwicklung von Stoffwechselwegen dienen.
Ein bemerkenswertes Beispiel für ein konvergent entwickeltes komplexes Naturstoffgerüst sind die Ipecac-Alkaloide. Diese von Monoterpenoiden abgeleiteten Tetrahydroisochinolin-Alkaloide kommen in den Ordnungen Cornales und Gentianales vor, die sich vor mindestens 100 Millionen Jahren getrennt haben. In unserer Arbeitsgruppe untersuchen wir die Biosynthese von Ipecac-Alkaloiden in Carapichea ipecauanha (Gentianales) und Alangium salviifolium (Cornales) in vergleichender Weise als Modell für konvergente Stoffwechselwege. Bemerkenswert ist, dass einige Brechwurzel-Alkaloide Brechreiz auslösen, weshalb beide Arten als Heilpflanzen bekannt sind: "Brechwurzelsirup", ein Extrakt aus den Wurzeln von C. ipecacuanha, war jahrzehntelang ein frei verkäufliches Brechmittel, während A. salviifolium in der traditionellen ayurvedischen Medizin als "Ankol" zur Behandlung von Darmparasitenbefall, Rheuma und vielen anderen Krankheiten bekannt ist.
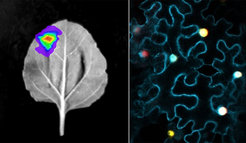
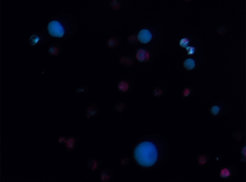
Wir haben die Stoffwechselwege in beiden Arten mithilfe klassischer Methoden zur Entdeckung von Stoffwechselwegen aufgeklärt, d. h. durch die Generierung von Genomik-, Transkriptomik- und Metabolomikdaten und die anschließende Rekonstitution der Stoffwechselwege in Nicotiana benthamiana sowie durch In-vitro-Enzymaktivitätstests mit rekombinant hergestellten Proteinen. In-silico-Ansätze wie phylogenetische Analysen und Proteinmodellvergleiche (alphafold2) werden eingesetzt, um die Enzyme des Stoffwechselweges zu vergleichen und herauszufinden, aus welchen Enzymfamilien des Primärstoffwechsels sie rekrutiert wurden. Darüber hinaus befassen wir uns mit dem wichtigen, aber bisher wenig untersuchten Aspekt der Evolution der Regulationsmechanismen von Stoffwechselwegen. So müssen beispielsweise die Genexpression in den Stoffwechselwegen sowie die subzelluläre Lokalisierung der Enzyme und die potenzielle Kanalisierung des Stoffwechsels koordiniert werden, um eine effiziente Produktion eines Naturprodukts zu erreichen. Daher vergleichen und kontrastieren wir auch die Genexpressionsmuster vom Gewebe bis hinunter zur einzelnen Zellebene in beiden Arten und analysieren die subzelluläre Lokalisierung und Protein-Protein-Interaktionen.
Darüber hinaus konzentrieren wir uns auf die Anwendung neuer Methoden zur Untersuchung von Stoffwechselwegen und deren Regulierung auf zelltypspezifischer Ebene. In Zusammenarbeit mit anderen Labormitgliedern und externen Mitarbeitenden führen wir Einzelzell-Metabolomik und Einzelzell-Transkriptomik durch, um besser zu verstehen, wie spezialisierte Stoffwechselwege auf der zelltypspezifischen Ebene organisiert sind.

Eine unabhängige Proof-of-Concept-Studie konzentrierte sich auf ein besseres Verständnis des Proteingehalts von Regulatoren zelltypspezifischer Prozesse, einschließlich, aber nicht beschränkt auf die Expression zelltypspezifischer Signalwege. Da der Nachweis von regulatorischen Proteinen mit geringer Häufigkeit immer noch eine große Herausforderung in der Einzelzellproteomik darstellt, verwenden wir die Protein-Näherungsmarkierung, um regulatorische Kernproteine aus verschiedenen Zelltypen aufzuspüren und zu analysieren. Diese Studie wurde an der Modellpflanze Arabidopsis thaliana durchgeführt, da sie leicht transformierbar ist und wesentliche Vorkenntnisse über zelltypspezifische Promotoren vorhanden sind.



